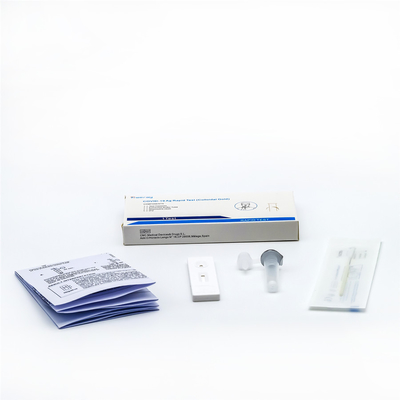
Produktbeschreibung: CER Antigen-schnelle Entdeckungs-Ausrüstung, Plastikantigen-Test-Ausrüstung
Antigen-ist schnelle Test-Ausrüstung schneller und weniger aufdringlich als ein Test der Polymerase-Kettenreaktion (PCR). Dieses makess es einfach, damit die Öffentlichkeit verwendet, um sich zu prüfen, wenn Sie gebraucht werden. Im allgemeinen Antigen-hat schnelles Test-Kind eine Empfindlichkeit (Fähigkeit eines Tests, Patienten mit der Krankheit zu identifizieren) von ungefähr 95% für Fälle mit höheren Virenlasten und eine Strecke der Besonderheit (Fähigkeit eines Tests, Patienten ohne die Krankheit zu identifizieren) 99.1%.As die Empfindlichkeit und die Besonderheit des Antigens schnelle Test-Ausrüstung verglichen mit PCR-Tests niedriger sind, wenn Sie schnelle Ausrüstung Test des Antigens prüfen, die zweimal positiv oder ungültig ist, das Sie mit einem bestätigenden PCR-Test verfolgen müssen. Sie sollten die Antigen-schnelle Test-Ausrüstung nicht wiederholen, selbst wenn Sie negatives im wiederholten Test prüfen, es sind möglicherweise ein falsches negatives Ergebnis und folglich müssen Sie einen bestätigenden PCR-Test anstreben. Poweray-Antigen-hat schnelle Test-Ausrüstungen die gute Leistung und mit hoher Empfindlichkeit, zum des Antigens am Anfangsstadium der Infektion zu ermitteln. Schneller Test der Hochleistung unmittelbaren Behandlungs- oder Isolierungsmaßnahmen ermöglichen, Getriebe herabzusetzen
Hauptkomponenten: Die Ausrüstung besteht Testkarten, Beispielpuffer und aus PUTZLAPPEN.
Testkarte: bestanden aus Aluminiumfolietasche, Trockenmittel, Teststreifen und Plastikkarte. Testblatt besteht saugfähigem Papier, Nitrozellulosefilm, Testauflage, klebender Auflage und aus Gummiblatt. t-Linie, die Nitrozellulosefilm mit nvvab 2019 umfasst (Testlinie), c mit Ziegemaus polyclonal AB (Qualitätssicherungslinie) und nvvab 2019. auf der Auflage
Beispielpuffer: Phosphat, Natriumnitrid, etc.
Produktanwendung:
Diese Ausrüstung wird für qualitative Entdeckung Vitros von coronavirus (Covid-19) menschlichem in pharyngeal oder in den Nasensekreten, sailva Proben benutzt.
Verwendet als Ergänzungstestindikator für vermutete Fälle neues coronavirus Nukleinfeuerprobenegativs oder in Verbindung mit Nukleinsäureprüfung in der Diagnose von vermuteten Fällen verwendet
Vorkehrungen:
1. Dieses Produkt wird für nur in-vitrodiagnose benutzt.
2. Dieses Produkt ist Wegwerf und kann nicht aufbereitet werden.
3. lesen Sie die Anweisungen sorgfältig vor Operation 3. und befolgen Sie ausschließlich die Reagensanweisungen.
4. Vermeiden Sie schwere Umweltbedingungen einschließlich Desinfektionsmittel 84, Natriumhypochlorit, Säure und Alkali oder Acetaldehyd, andere hohe Konzentrationen von Schadgasen und von Staub, etc., das Labor sollen disinfed
5. Alle benutzten Proben und Reagenzien werden als möglicherweise ansteckende Materialien angesehen und werden in Übereinstimmung mit lokaler Gesetzgebung behandelt.
6. Gebrauchsreagenzien innerhalb des Gültigkeitszeitraums zeigten in der Umverpackung an. Benutzen Sie die Testkarte so bald wie möglich nach Abbau von der Aluminiumfolietasche.
Kontrollverfahren:
- Entfernen Sie die Folie von der Spitze des Extraktionspufferrohrs
- Öffnen Sie das Putzlappenpaket am Stockende
- Fügen Sie leicht den Putzlappen in das Nasenloch ein und die Spitze des Putzlappens sollte eingefügt werden Zoll 1/2-3/4 weg von dem Rand des Nasenloches
- Rollen Sie den Putzlappen entlang der Schleimhaut innerhalb des Nasenloches 5mal und ungefähr 15 Sekunden nehmen, um das Exemplar zu sammeln
- Fügen Sie den Repräsentativputzlappen in den Beispielpuffer ein
- Wirbeln das Rohr für 30 Sekunden
- Drehen Sie den Putzlappen 5mal beim Zusammendrücken des Rohrs
- Entfernen Sie den Putzlappen beim Zusammendrücken des Rohrs
- Bedecken Sie den Emitter
- Addieren Sie 2 Tropfen, um die behandelte Probe zum ladenden Brunnen der Testkarte zu extrahieren und den Timer dann zu beginnen
- Vor dem Ablesen der Ergebnisse verlassen Sie bei Zimmertemperatur für 15 Minuten. Das Ergebnis ist nach 20 Minuten ungültig
Ausführliche Erklärung von Testergebnissen:

Beschränkung der Prüfmethode:
1. Dieses Produkt wird für die qualitative Prüfung und nur für unterstützte in-vitrodiagnose benutzt.
Produkt 2.This beantragt Nasenproben. Andere Beispielart Ergebnisse ist- möglicherweise ungenau oder ungültig.
3. fügt passend Proben für die Prüfung hinzu. Zu große oder zu kleine Mustergröße möglicherweise führt zu ungenaue Ergebnisse.
4.It sollte nicht die einzige Basis für klinische Studien und Behandlung sein. Die endgültige Diagnose kann nach einer umfassenden Bewertung von allem klinischen und von Versuchsergebnissen gemacht werden.
Wenn irgendeine Frage, pls Kontakt Anmut durch E-Mail: grace@poweray.com.cn, Mobile/wechat: 13310839332

 Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten!
Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten! Bitte überprüfen Sie Ihre E-Mail!
Bitte überprüfen Sie Ihre E-Mail!  Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten!
Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten! Bitte überprüfen Sie Ihre E-Mail!
Bitte überprüfen Sie Ihre E-Mail!