Produktbeschreibung: Antigen-schnelle Test-Ausrüstung
COVID-19 AG schneller Test ist ein seitlicher Fluss Immunoassay, der für die qualitative Entdeckung des Nucleocapsid-Antigens von SARS-CoV-2 in den Nasenrachenraumputzlappen von den Einzelpersonen bestimmt sind, die von SARS-COV-2 von ihrem Gesundheitsvorsorger innerhalb der ersten 7 Tage des Symptomanfangs vermutet werden, oder für Siebung von Einzelpersonen ohne Symptome oder andere Gründe, Infektion SARS-COV-2 zu vermuten, falls zutreffend.
Positive Ergebnisse zeigen das Vorhandensein von Virenantigenen an, aber klinische Wechselbeziehung mit Patientenanamnese und anderen Diagnoseinformationen ist notwendig, um Infektionsstatus zu bestimmen. Positive Ergebnisse streichen nicht bakterielle Infektion oder Mitinfektion mit anderen Viren durch. Das Mittel ermittelte ist möglicherweise nicht die bestimmte Krankheitsursache. Labors innerhalb der Vereinigten Staaten und seiner Gebiete werden angefordert, um allen positiven Ergebnissen das passende allgemeine Gesundheitsamt zu berichten.
Negative Ergebnisse sollten behandelt werden, wie vermutlich und streichen Infektion nicht SARS-CoV-2 durch und sollten nicht als die einzige Basis für Behandlung oder geduldige Unternehmensentscheidungen, einschließlich Infektionskontrolleentscheidungen verwendet werden. Negative Ergebnisse sollten im Rahmen der neuen Belichtungen eines Patienten, der Geschichte und des Vorhandenseins von klinischen Zeichen und von Symptomen betrachtet werden, die mit COVID-19 in Einklang sind, und mit einer molekularen Probe, für geduldiges Management gegebenenfalls bestätigt werden.







Produktverwendung:
Diese Ausrüstung wird für qualitative Entdeckung Vitros von coronavirus (Covid-19) menschlichem in pharyngeal oder in den Nasensekreten, sailva Proben benutzt.
Verwendet als Ergänzungstestindikator für vermutete Fälle neues coronavirus Nukleinfeuerprobenegativs oder in Verbindung mit Nukleinsäureprüfung in der Diagnose von vermuteten Fällen verwendet
Hauptkomponenten:
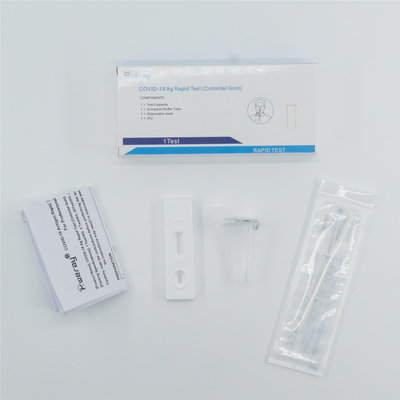
Die Ausrüstung besteht Testkarten, Beispielpuffer und aus PUTZLAPPEN.
Testkarte: bestanden aus Aluminiumfolietasche, Trockenmittel, Teststreifen und Plastikkarte. Testblatt besteht saugfähigem Papier, Nitrozellulosefilm, Testauflage, klebender Auflage und aus Gummiblatt. t-Linie, die Nitrozellulosefilm mit nvvab 2019 umfasst (Testlinie), c mit Ziegemaus polyclonal AB (Qualitätssicherungslinie) und nvvab 2019. auf der Auflage
Beispielpuffer: Phosphat, Natriumnitrid, etc.
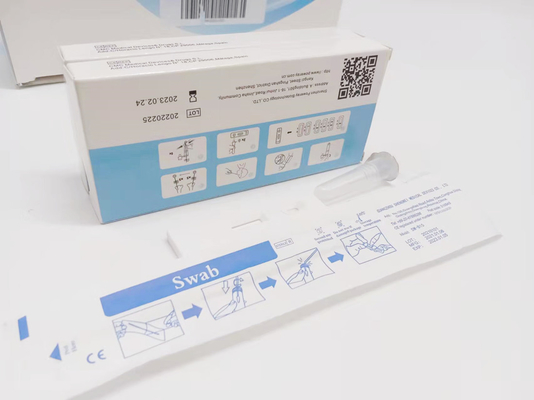
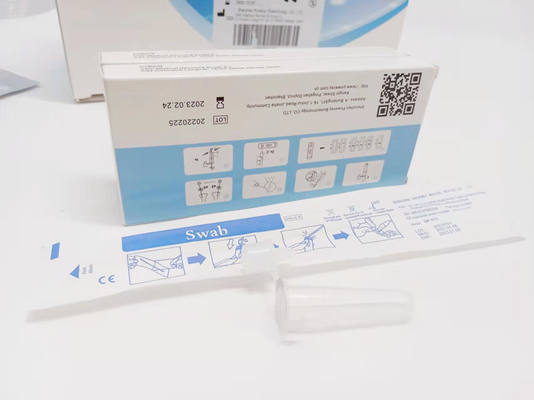
Testverfahren:
- Entfernen Sie die Folie von der Spitze des Extraktionspufferrohrs
- Öffnen Sie das Putzlappenpaket am Stockende
- Fügen Sie leicht den Putzlappen in das Nasenloch ein und die Spitze des Putzlappens sollte eingefügt werden Zoll 1/2-3/4 weg von dem Rand des Nasenloches
- Rollen Sie den Putzlappen entlang der Schleimhaut innerhalb des Nasenloches 5mal und ungefähr 15 Sekunden nehmen, um das Exemplar zu sammeln
- Fügen Sie den Repräsentativputzlappen in den Beispielpuffer ein
- Wirbeln das Rohr für 30 Sekunden
- Drehen Sie den Putzlappen 5mal beim Zusammendrücken des Rohrs
- Entfernen Sie den Putzlappen beim Zusammendrücken des Rohrs
- Bedecken Sie den Emitter
- Addieren Sie 2 Tropfen, um die behandelte Probe zum ladenden Brunnen der Testkarte zu extrahieren und den Timer dann zu beginnen
- Vor dem Ablesen der Ergebnisse verlassen Sie bei Zimmertemperatur für 15 Minuten. Das Ergebnis ist nach 20 Minuten ungültig
Ausführliche Erklärung von Testergebnissen:

Produktleistungsindikator:
Die coronavirus (Covid-19) Antigen-Entdeckungsausrüstung wurde benutzt, um 60 positive Fälle mit einer Empfindlichkeit von 95% von 170 negativen Exemplaren, die mit der Antigen Covid-19 detectior Ausrüstung geprüft wurden, 168 zu ermitteln waren negativ, mit einer Besonderheit von 99,1%






 Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten!
Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten! Bitte überprüfen Sie Ihre E-Mail!
Bitte überprüfen Sie Ihre E-Mail!  Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten!
Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten! Bitte überprüfen Sie Ihre E-Mail!
Bitte überprüfen Sie Ihre E-Mail!